中3の理科について質問です。 問題 濃度5%の塩酸cm3に 濃度7%の水酸化ナトリウム水溶液を15cm3加えると中性になった (1)濃度10%の塩酸cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか →答えは 30cm3 (2)濃度5%の塩酸40cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか理科用語を使って説明することができていないことがわか 3/4 空気の体積変化について 中3年「水溶液とイオン」 中3年「酸・アルカリとイオン」中 中3 理科 化学変化とイオン 化学変化とイオン(pdf37キロバイト) r2;
中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス
中 3 理科 イオン 体積
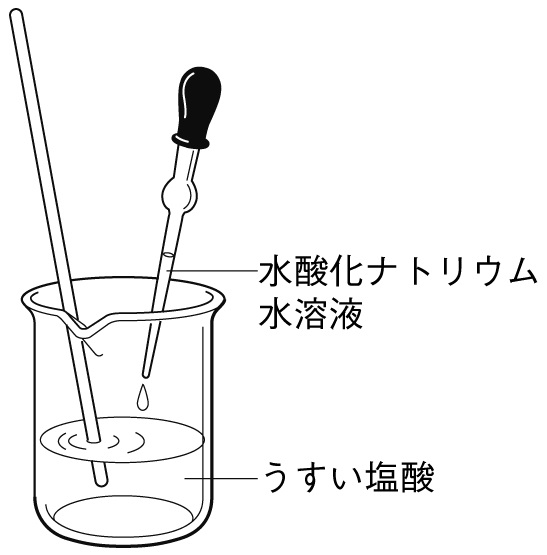
中 3 理科 イオン 体積- 中和とは 塩酸のような酸性の水溶液と、水酸化ナトリウムのようなアルカリ性の水溶液を混ぜると、お互いの性質を打ち消し合う反応である中和が起こります 。 このとき酸性の水溶液中にある 水素イオンH⁺ と、アルカリ性の水溶液中にある 水酸化物イオンOH⁻ が結びつき 水H₂O が生じます。 また、それ以外の 酸の陰イオン と アルカリの陽イオン が結びつき イオン♪中和の問題です。 中3理科の定期テスト対策! こんにちは。 小幡校&貴船校の原田です。 水酸化ナトリウムの粒を指ですべすべしていたら指紋がなくなりました。 中3理科より問題です。 ある濃度の塩酸25㎤とある濃度の水酸化ナトリウム水溶液30㎤を混ぜたら完全に中和した。 次の問いに答えなさい。 (1)この塩酸75㎤を完全に中和する水酸化



中3理科 中和の計算問題 Examee
中和の計算問題 無料で使える中学学習プリント 中3理科中和の実験・イオン数のグラフ Examee 中3理科 生物植物と動物の有性生殖・無性生殖 一発解決! 中3理科化学電池とイオンについて;中3です。「電子のやり取り」の法則って? 中3です。「化学電池」のしくみが分かりません。 中3です。「酸性」「アルカリ性」とイオンの関係は? 中3です。「中和」の意味が分かりません。 中3
①⑴A液10cm3に対してB液が8cm3 〈この状態で中和している〉 A液がcm3になっていて、中和の時から2倍になっているので、B液も2倍する。 なので、80×2=16 となります。 ⑵C液がの濃度が2倍になっただけで量は変わらないので⑴と同じように なので、80×2=16 となります。 ②⑴A液は水素イオン イオンの濃度と体積の関係 中3の理科について質問です。 問題 濃度5%の塩酸cm3に 濃度7%の水酸化ナトリウム水溶液を15cm3加えると中性になった ①濃度10%の塩酸cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか →答えは 30cm3 ②濃度5%の塩酸40cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか →答中3理科塩化銅水溶液の電気分解の定期テスト対策問題 🚀 この方法で,銅イオンを沈殿させれば、廃液の体積を小さくすることができます。 15
中3理科イオン酸とアルカリ、中和まとめと問題 酸は水に溶けると酸性、アルカリは水に溶けるとアルカリ性になる物質のことです。 酸性の水溶液は水素イオン、アルカリ性の水溶液は水酸化物イオンが含まれています。 酸性の水溶液とアルカリ性の水溶液を混ぜると中和がおこり、水溶液は中性に近づいていきます。 酸やアルカリにはいったいどんな物質が中3化学 17年10月9日 / 最終更新日時 18年2月10日 進学研究室 中3化学 塾の見解 中3化学 イオン(解答例) ①同じ濃度で体積を3倍にする ②同じ体積で濃度を2倍にする ③水を加えて体積を3倍にする。 これは、 塩酸中の陽イオンである水素イオン H⁺ が陰極に、陰イオンである塩化物イオン Cl⁻ が陽極に引き寄せられる ためです。 陰極から発生する水素と、陽極から発生する塩素の体積は同じですが、実際には陽極から発生する塩素の方が少なくなります。



中3理科 期末テスト 化学電池の問題 ブログ アビット




中3 理科 中3 33 太陽系の天体 Youtube
で,塩酸中には水素イオンと塩化物イオンが含まれています。 体積は気体の分子数に比例する」という性質がある。 見本 高校受験コース 本科 中3理科 要点学習答えは100cm 3 ② 塩酸の濃さを2倍にして体積も2倍になっているので、中のイオンの数は 4(倍) になっています。 中和するためのNaOH水溶液の体積も4倍必要です。 50(cm 3 )=0(cm 3 ) 答えは0cm 3 ③ 水でどれだけうすめても中のイオンの数はもとのままです。(3) 次の化学反応式から、濃度が等しいHCl 水溶液とNaOH 水溶液が中和する時の体積の比を、最 も簡単な整数の比で表しなさい。 HCl + NaOH → NaCl + H 2 O ( ) (4) 3この実験で用いた濃度のHCl 水溶液140cm を中和するには、この実験で用いたNaOH 水溶液




中学理科 中学で習う実験 観察の一覧 入試でよく出る編 中学生勉強サイトあかね先生



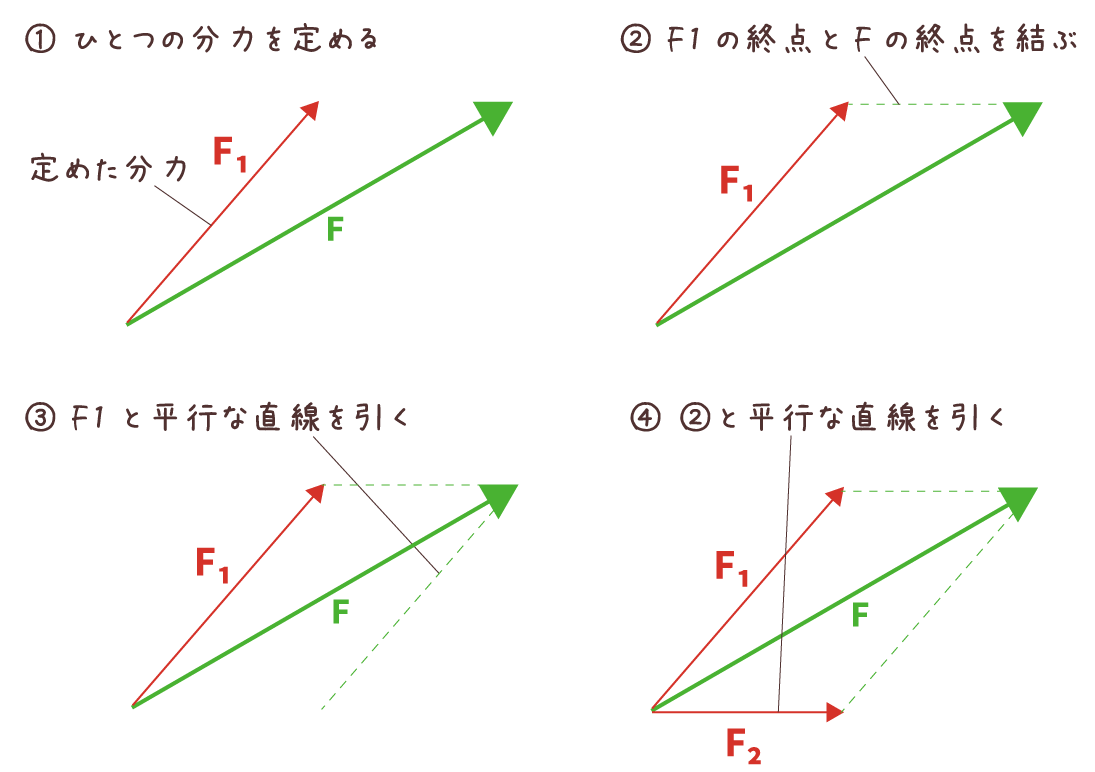
令和3年度1学期中間テスト予想問題 中3理科 力の合成と分解 浮力と水圧 速さ 赤城 ᐡᐤᐡ
イオンの濃度と体積の関係 中3の理科について質問です。 問題 濃度5%の塩酸cm3に 濃度7%の水酸化ナトリウム水溶液を15cm3加えると中性になった (1)濃度10%の塩酸cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか →答えは 30cm3 (2)濃度5%の塩酸40cm3の場合 濃度7%の水3 とイオン 化学変化と電池 水溶液の電気伝導性、中和反応、電池の仕組みをイオンモデルと関連付けて考 える。 校 校 種種 学 年 学習内容 単元の主な理科の着目する点 ・考え方 小 校 6 3 物と重さ 形や体積 重さを比較する 中学3年理科。中和について学習します。 レベル:★★★☆ 重要度:★★★☆ ポイント:H⁺、OH⁻、Na⁺、Cl⁻の数の変化授業用まとめプリントは下記リンクよりダウンロード!授業用まとめプリント「中和と塩」授業用まとめプリント「中和と




気体の性質と特徴一覧表 の無料学習プリント 中学理科 中学受験 Yattoke 無料プリント
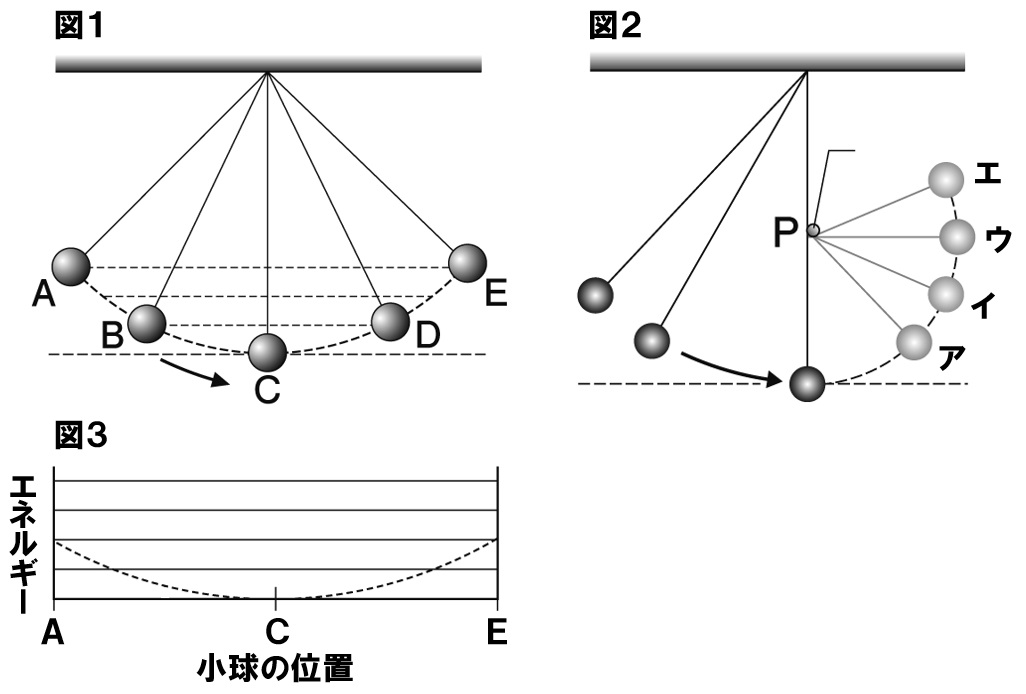



中3理科 仕事とエネルギー テスト対策問題 Examee
You're signed out Videos you watch may be added to the TV's watch history and influence TV recommendations To avoid this, cancel and sign in to on your computer Cancel Confirm資料2:空気・水の学習内容系統 学習指導要領 理科 (小・中学校) 「空気」についての内容 小学第 3学年 風やゴムの働き ア風の力は,物を動かすことができること。 第 4学年 空気と水の性質理科学習指導案(第3学年) える必要がある。水溶液の濃さと体積という二つの要素を基に、イオンのモデルを操作することで水 第10時 まとめ イオン数に着目した中 実験の結果とモデルを 観察、実験を行い、濃度



分からない問題があるので教えてください 中3理科イオンです Yahoo 知恵袋




中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス
英検cbtを初めて受ける方必見!英検cbt当日の流れ 塾長の英検準一級勉強方法 年夏期講習について 開校時間3 小・中学校の理科教育の接続を踏まえた理科授業づくりとの関わり ⑴ 粒子概念に関する微視的な視点での接続 第1分野で化学についての学習内容は、小・中学校を通して「粒子」を柱として構 成されて 中3 理科 2学期 期始め・実力テスト 練習問題⑴ テーマ: 公立高校入試 中学3年 全国公立高等学校入試問題改 理科 水溶液とイオン 1.図のような装置でうすい塩酸の電気分解を行うと,陽極と陰極からそれぞれ気体が発生した。 ⑴塩酸




中3 水溶液とイオン 中学生 理科のノート Clear



中三理科の中和の濃度と体積の問題です 大問4が答えの解説を見てもわか Yahoo 知恵袋
令和3(21)年度用 理科 教科書QRコンテンツ 中学校 啓林館 お問い合わせ 教科書の内容に即したデジタルコンテンツを多数ご用意しています。 (3学年計 約390コンテンツ:QRコード約310箇所) 基礎的・基本的な知識・技能を確実に習得するための水溶液が同濃度の場合,同体積が必要 であったことを確認する。 ・ 水素イオンと水酸化物イオンのモデル 図を用いて中和について確認する。 ・ 基準となる水酸化ナトリウム水溶液10 mLの中には水酸化物イオンが4個含ま れていると仮定する。〈理科基礎シート〉 加えた塩酸の体積とまぜた水溶液のある2つのイオンの数の関係を表したものです。 (1)BTB溶液が黄色になるまでの色の変化を書きなさい。 (3)図4中のA・Bのイオンをイオン式で書きなさい。




中学理科の重要用語まとめ 高校入試よく出る編 中学生勉強サイトあかね先生
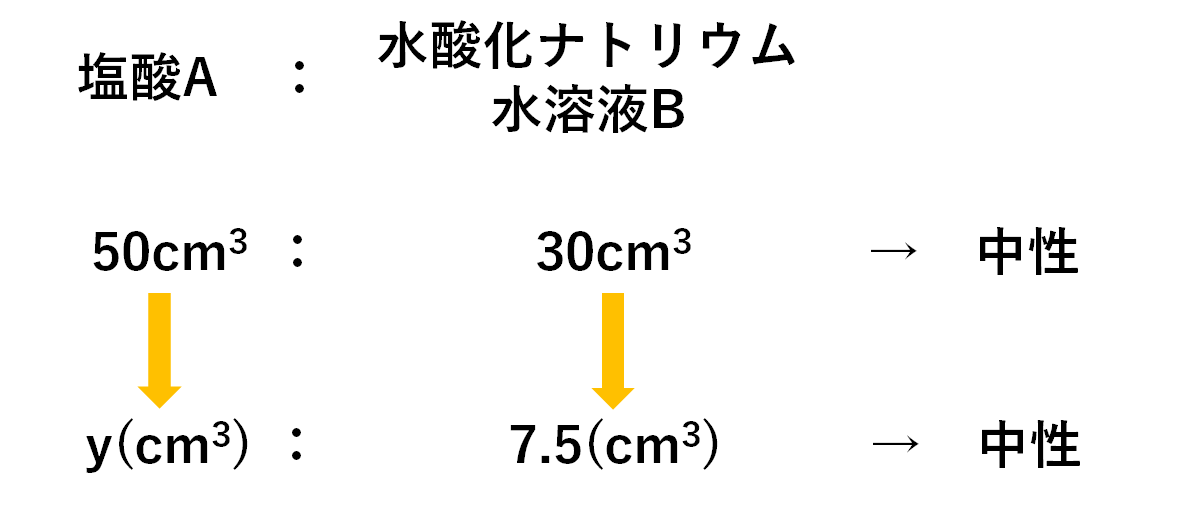



中3化学 中和の量的関係 中学理科 ポイントまとめと整理
中3で学習するイオン・中和の「中和の量的関係」についての計算問題集です。 PDFファイルの販売になります。 中学3年生以上向けの内容になっています。 入試や模試などに向けた復習用教材としても使用できます。 収録内容 問題番号1 塩酸または水酸化ナトリウム水溶液を中性にするのにFdData中間期末:中学理科3年化学 イオン数の変化 パソコン・タブレット版へ移動 塩酸+水酸化ナトリウム 問題(前期期末 ) うすい塩酸にうすい水酸化ナトリウム 水溶液を加えていくとき,水溶液中の① 水素イオンの数,②水酸化物イオンの数, 中3の理科について質問です。 問題 濃度5%の塩酸cm3に 濃度7%の水酸化ナトリウム水溶液を15cm3加えると中性になった (1)濃度10%の塩酸cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか →答えは 30cm3 (2)濃度5%の塩酸40cm3の場合 濃度7%の水酸化ナトリウム水溶液は何cm3入れたら中性になるか




中3理科 中和の計算問題 Examee




理科 3 平成31年度埼玉県公立高校入試問題予想 埼玉新聞
問4 2%の塩酸と水酸化ナトリウム水溶液が完全に中和するときの体積比は,上の表より,5:15=10:3である。 したがって,10:3=350: x というイオン式 理由 3 実験後、C液~F液の4種類の液をすべて混ぜ合わせた。この液を中性にするためには、水酸化 ナトリウム水溶液と塩酸のどちらを何cm3加えれば良いか。 を cm3加える。 霧島市「今週の1問」 (中3)(理科)(10)月(26)日版中3化学 17年10月8日 / 最終更新日時 18年2月10日 進学研究室 中3化学 塾の見解 中3化学 イオン ①同じ濃度で体積を3倍にする ②同じ体積で濃度を2倍にする ③水を加えて体積を3倍にする。
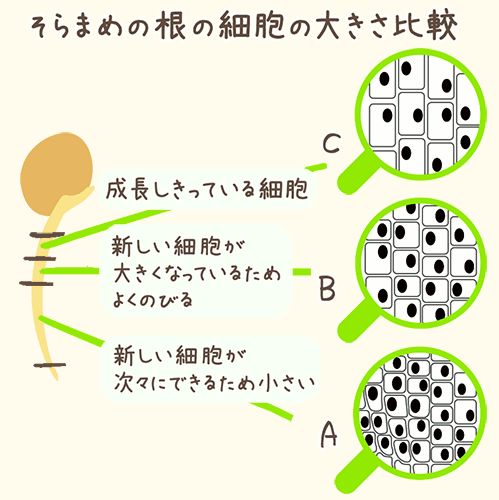



中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス




中3理科 イオン 酸とアルカリ 中和まとめと問題
中3理科で学ぶ「中和とイオン」のテストによく出る問題(中和とイオン)を学習しよう! 酸・アルカリと中和の問題を見る > すべての授業の「要点まとめノート」「問題・解答」をPDF無料ダウンロードできる 学校で使っている教科書にあわせて勉強できる わからないところを質問できる 会員登録をクリックまたはタップすると、 利用規約・プライバシー中性の水溶液の場合、pHの値は 7 になります。 水溶液の性質を表す単位がpHで、7が中性、7より小さいと酸性、7より大きいとアルカリ性でした。 図③を見ると、 BTB溶液が黄色になった と書いてあります。 つまり水溶液は アルカリ性 ということですね。 (2)は、水溶液のpHが大きい順に①②③を並び替える問題です。 先ほども説明しましたが、 pHが7だと中性、7より 前期中間テスト 中3理科イオン・電気分解のコツとは?! 岐阜県各務原市の学習塾、ナビ個別指導学院鵜沼校のブログ紹介。小学生・中学生・高校生を対象にした英語・国語・数学・理科・社会などの勉強法や、中学受験・高校受験・大学受験の情報を紹介しています。




楽天ブックス 自由自在中学理科 平成28年新装 1分野 2分野 伊藤久雄 本




中学理科 水の電気分解の確認問題 Irohabook
中3理科 2学期以降 新出単元演習 水溶液とイオン① 基礎クラスは1⃣2⃣3⃣4⃣7⃣8⃣9⃣🔟をやれる範囲で解くこと。 問1 塩化銅が水に溶 と けてイオンに分かれるようすを,化学式とイオン式を使って表しなさい。FdData中間期末:中学理科3年化学 中和の計算問題 パソコン・タブレット版へ移動 問題(2学期中間) ある濃度のうすい塩酸15cm 3に,ある 濃度のうすい水酸化ナトリウム水溶液を 10cm3加えたときに,過不足なく中和が おこり,混合液は中性になった。(a)H (b)Cl (c)OH (d)Na (e)NH 4 (f)Mg 2 (g)SO 4 2 (h)NO 3A 陽極から発生する塩素は水に溶けやすいので、気体の体積の少ないAから発生しているのが塩素と考えられるから。 陰極の気体(a,e,g,j) 陽極の気体(f,h,i) 2HCl→H 2 Cl 2
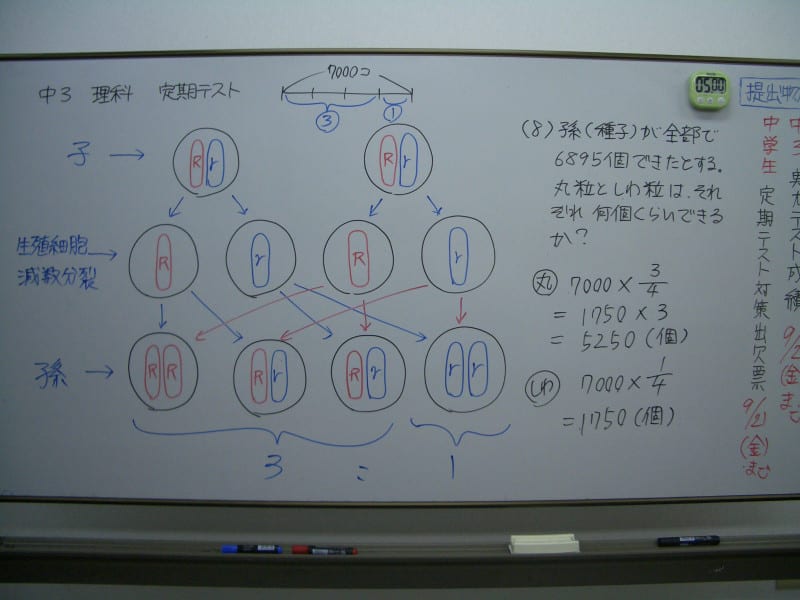



中3理科 篠津中定期テスト対策 遺伝の計算 ブログ アビット
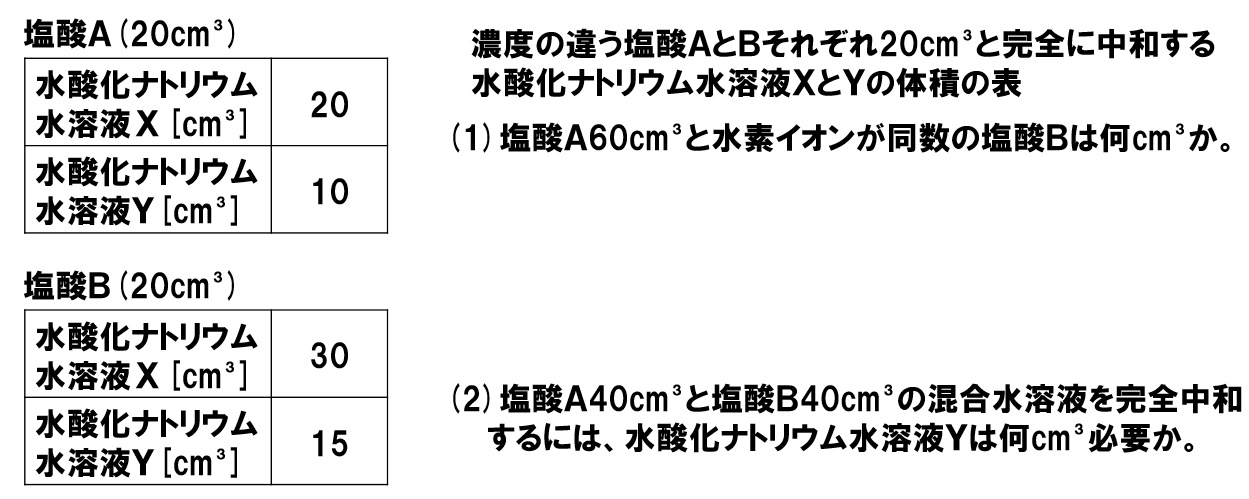



中3理科 完全中和の計算 Pikuu
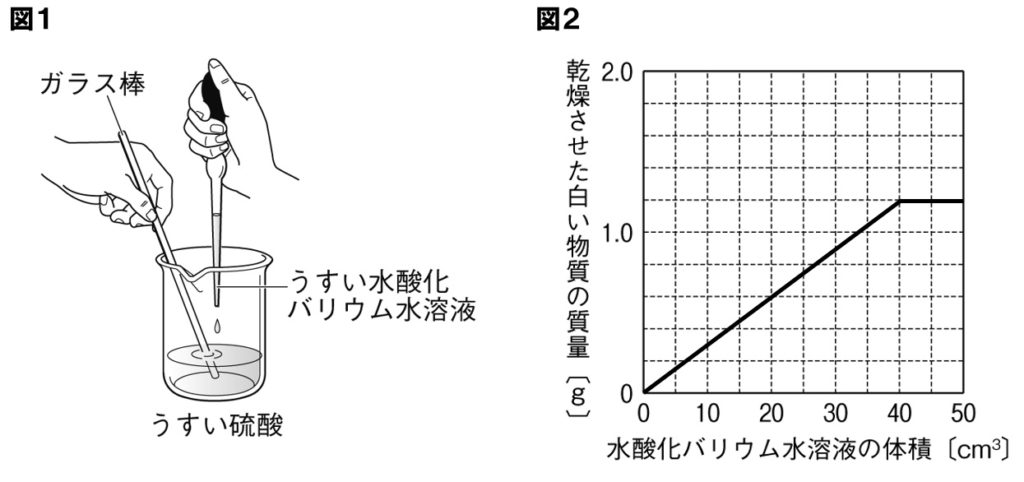
(4) 実験1の水酸化バリウム水溶液150cm 3 に水を混ぜて0cm 3 にしたので、1500=34 この比が同数のイオンを含む実験1と2の水酸化バリウム水溶液の体積比となる。 実験1で硫酸cm 3 に対して過不足なく反応した水酸化バリウム水溶液は30cm 3 であった。これと同数のイオンを含む実験2の水酸化バリウム水溶液をxとすると中3理科中和と濃度体積の問題です。助けてください。大問1の(1 気相濃度と水溶液の濃度の計算について 環境Q&A|EICネット;塩酸の体積はいつも80cm3。水酸化ナトリウム水溶液を 50cm3 加えたときに完全中和するから, 塩酸 + 水酸化ナトリウム水溶液 → 食塩 80cm 50cm 63 3 g となる。 〔塩酸80cm3〕 また,完全中和したあとには,水酸化ナトリウム水溶




印刷 中3 理科 イオン式 ニスヌーピー 壁紙
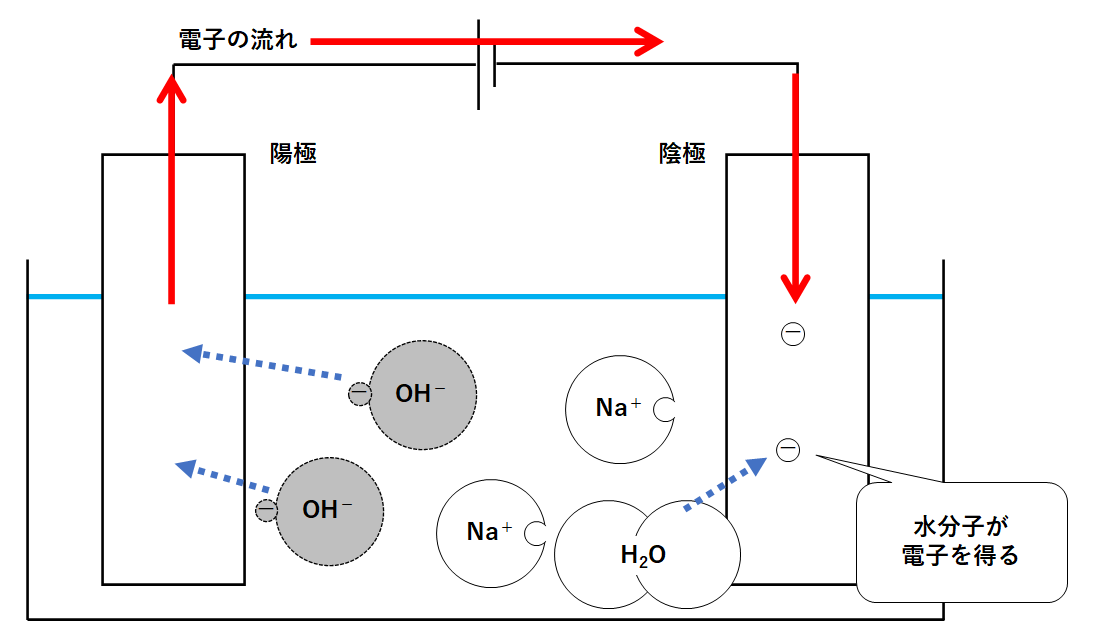



中3化学 水の電気分解 中学理科 ポイントまとめと整理



中3理科の科学の計算です 1 をお願いしますなぜ 塩酸の Yahoo 知恵袋
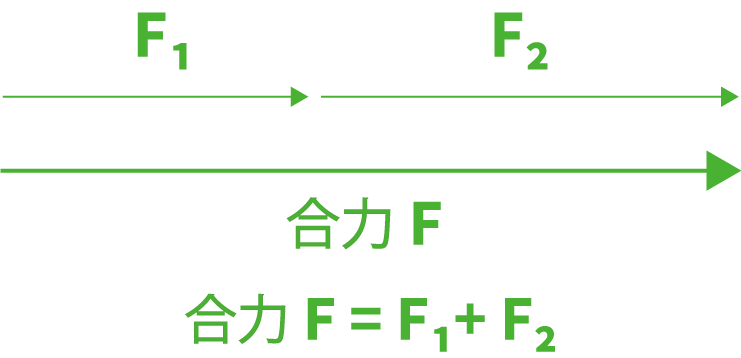



中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス




イオン 中和の問題です 中3理科の定期テスト対策 カシマブログ 名古屋の学習塾 鹿島塾




理科 3 平成31年度埼玉県公立高校入試問題予想 埼玉新聞




理科の中和と濃度 体積の所なんですけどよく分かんないです Clear




中1理科 密度の表し方 映像授業のtry It トライイット
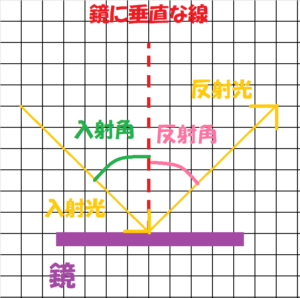



中学校理科の公式一覧




中学3年中和と濃度 体積の計算について 大問1と2はかろうじて理解出 中学校 教えて Goo




マイスタディガイド 中学理科




中学校理科の公式一覧



中3理科 イオンの勉強で色々ややこしくなってしまったのでまとめたのですが Yahoo 知恵袋



濃度と体積




理科 中3 9 イオンの移動 Youtube




9月19日更新 中3理科 毎年質問が多い問題 学校のワークより 成績 上がってます 根城学習塾 八戸市




中学 理科 天気 授業実践記録 理科 天気図作成による 天気 の単元のまとめと発展的な学習 Amp Petmd Com




理科の偉人一覧 中学生向け




中3理科 化学変化とイオン 2学期期末テスト 赤城 ᐡᐤᐡ



ダウンロード済み 中3 理科 イオン 計算 中3 理科 イオン 計算




楽天ブックス わかるをつくる 中学理科問題集 学研プラス 本
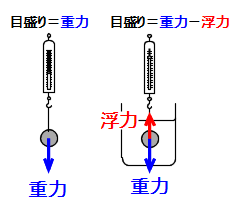



Science 浮力 ふりょく の基礎 基本 中学理科 働きアリ



Center Esnet Ed Jp Wysiwyg File Download 22 4500



印刷 中3 理科 イオン式 ニスヌーピー 壁紙



Http Www Mct Ne Jp Users Koavc Kon1 Data Jh3 Sc 05 Pdf




年度用 中学校理科教科書内容解説資料 未来へひろがるサイエンス




中和の計算問題 無料で使える中学学習プリント




中和の計算問題 無料で使える中学学習プリント
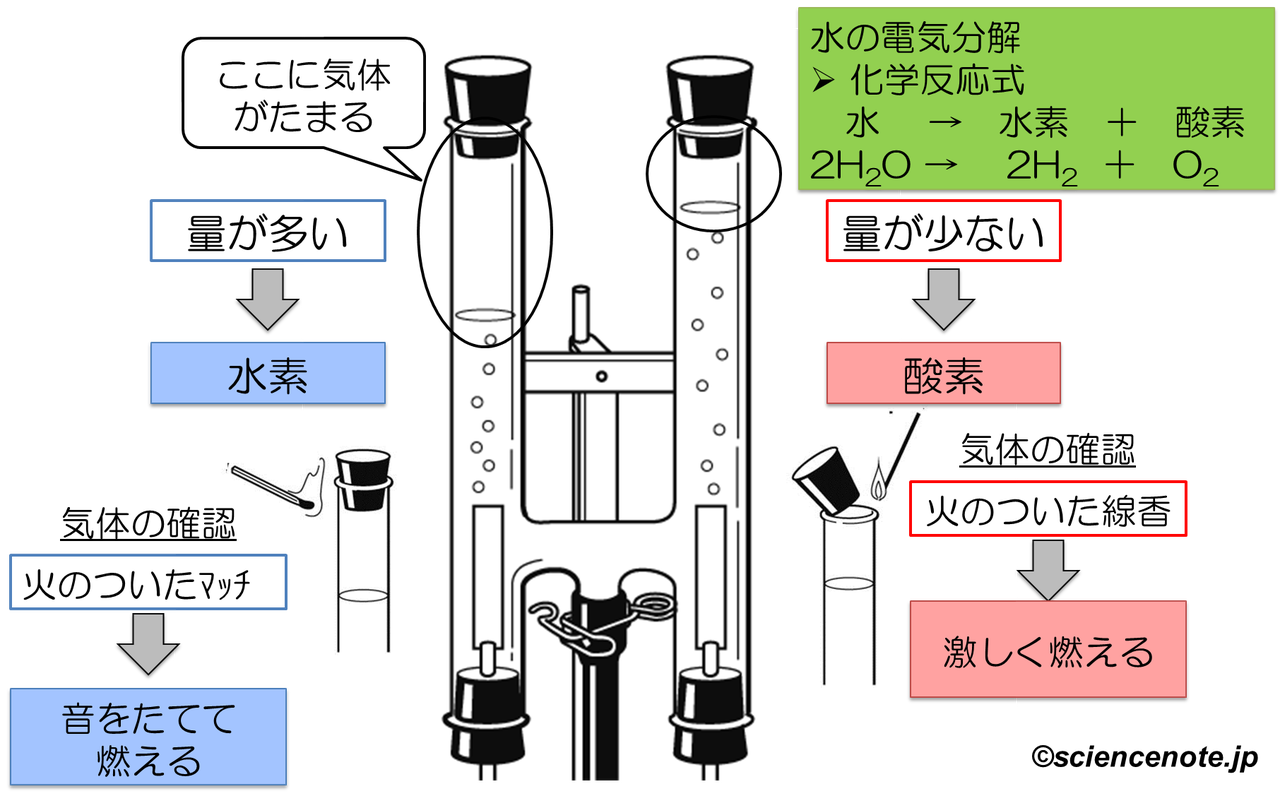



中2化学 水の電気分解 Hiromaru Note




ボード 学習ノート のピン




中3理科 定期テスト範囲 中和 ブログ アビット
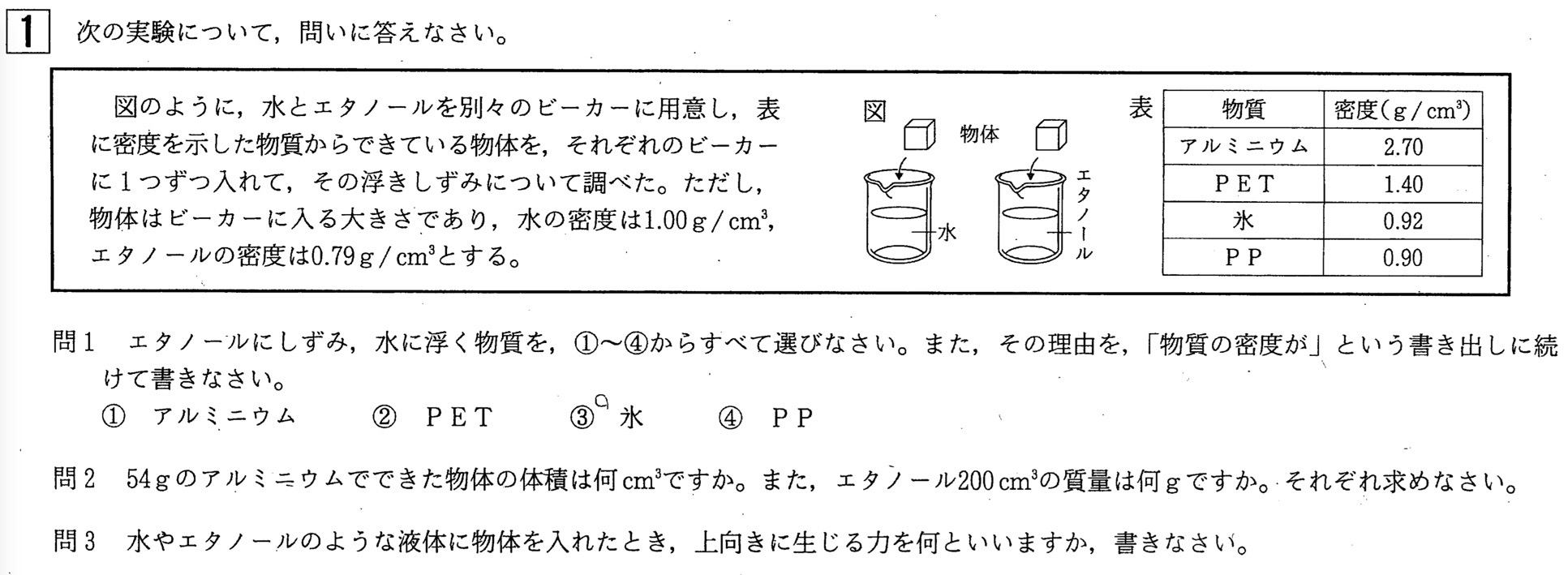



年過去問 中学3年北海道学力テスト総合a 理科 の問題 解答 答え 詳しい解説を全て公開します 家庭教師のsora
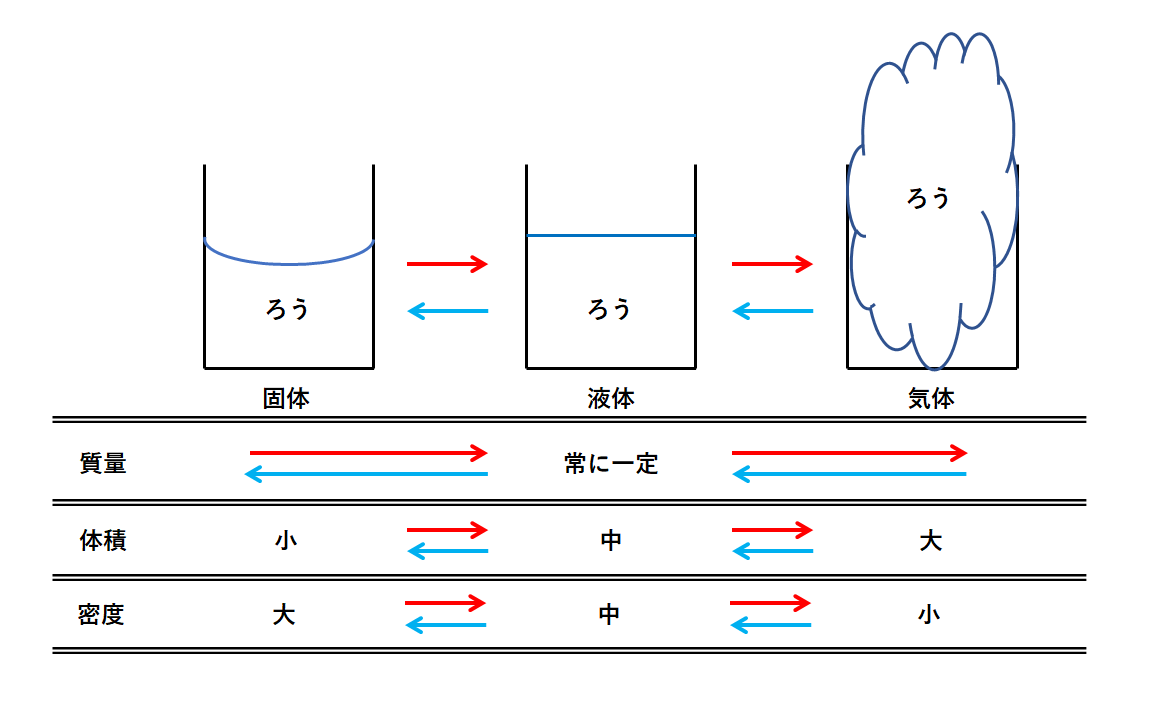



中1化学 状態変化 中学理科 ポイントまとめと整理




一問のみ質問です Clear




高校入試 中3理科 中和とイオン エネルギー 天体 実力テスト用 赤城 ᐡᐤᐡ
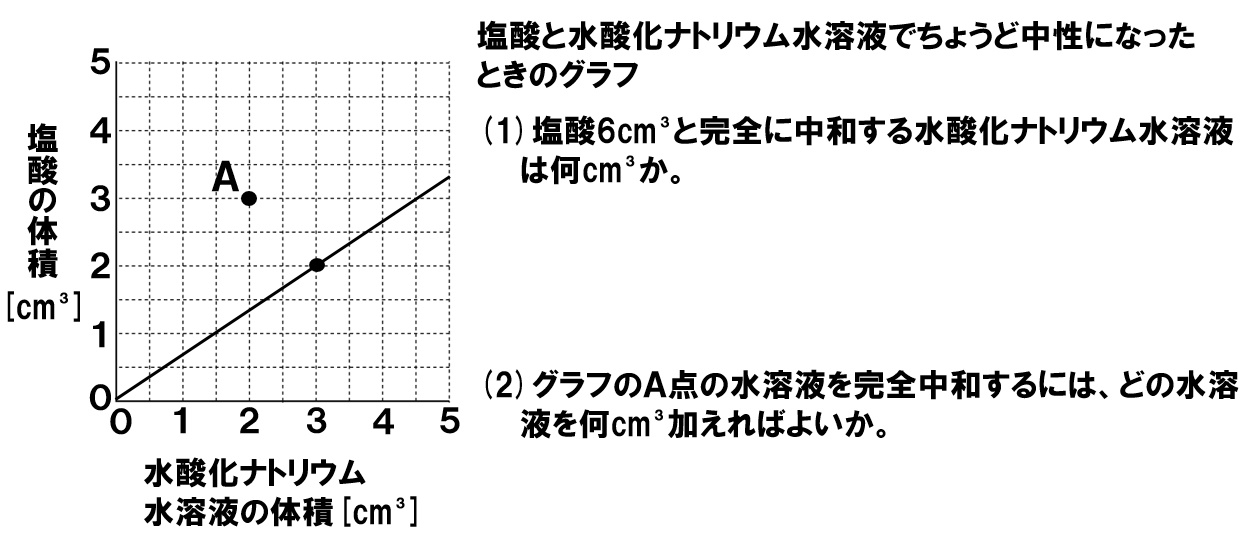



中3理科 完全中和の計算 Pikuu



濃度と体積
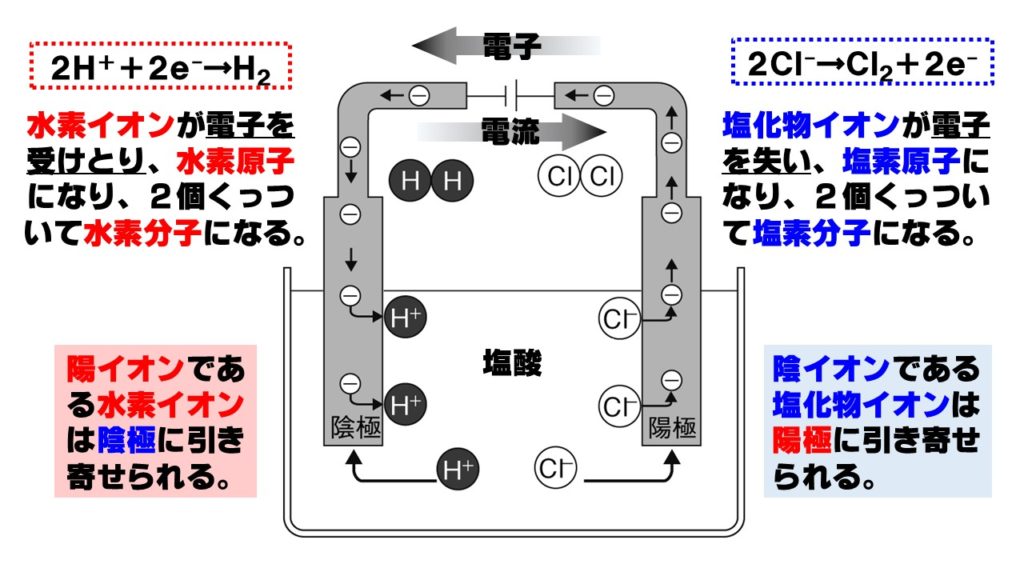



中3理科 塩酸の電気分解のポイント Examee
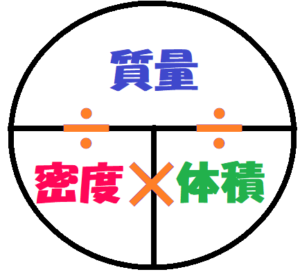



中学校理科の公式一覧
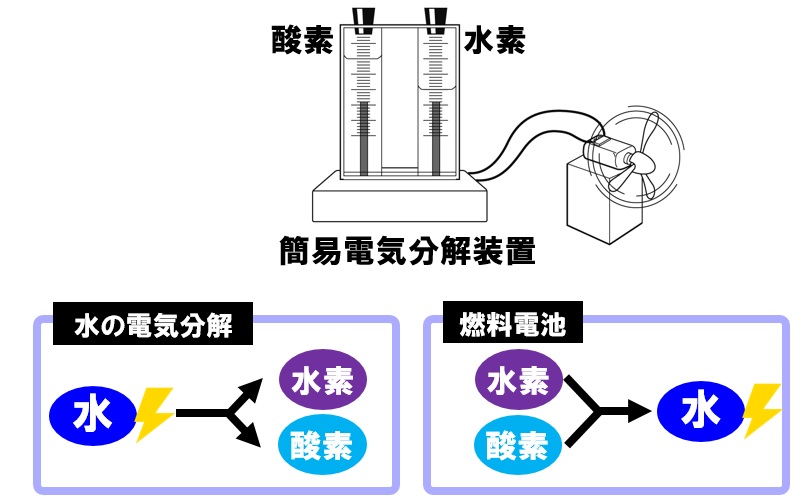



中3理科 燃料電池のポイント Examee



3




夏まとめ 中学理科公式まとめ 中学生 理科のノート Clear
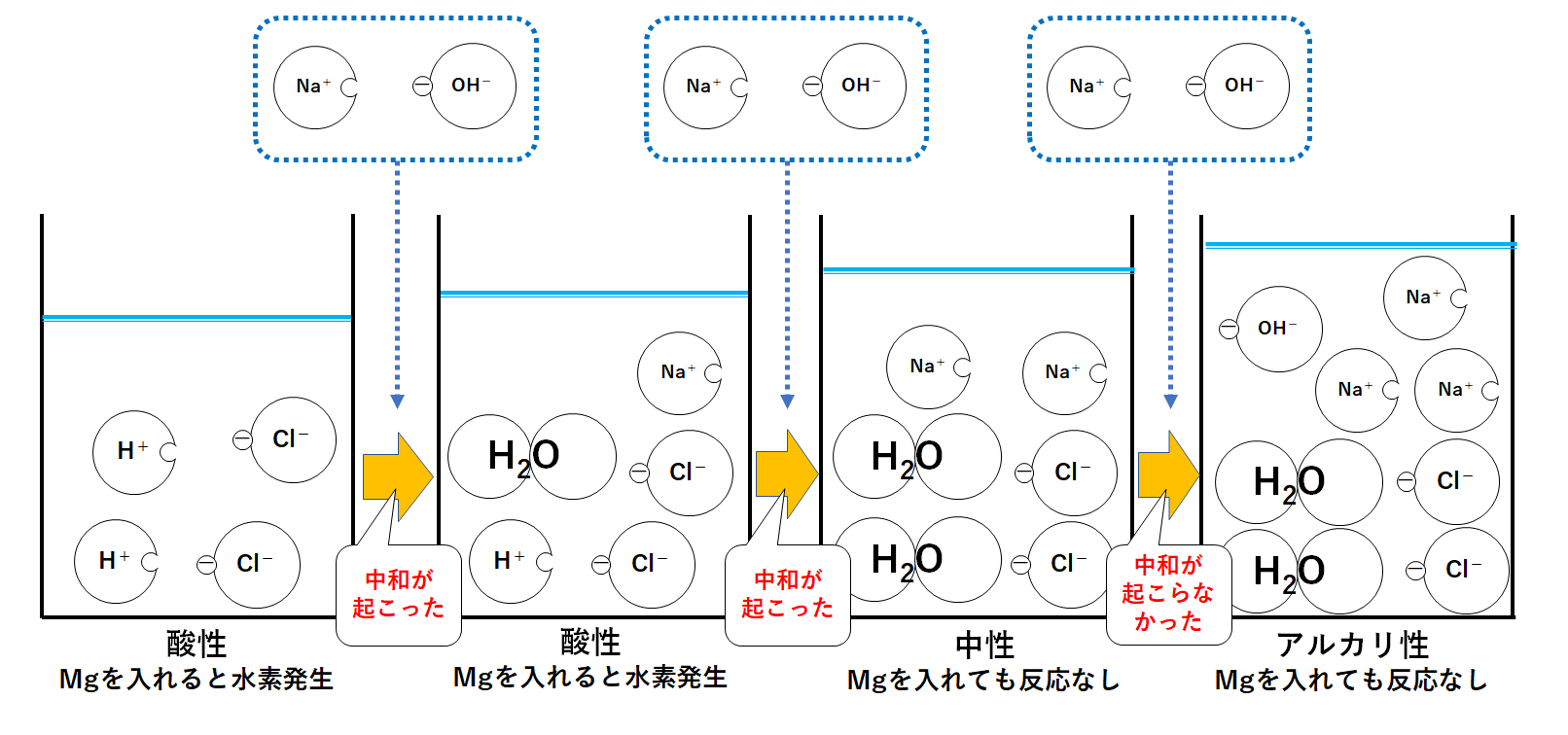



中3化学 中和反応 中学理科 ポイントまとめと整理
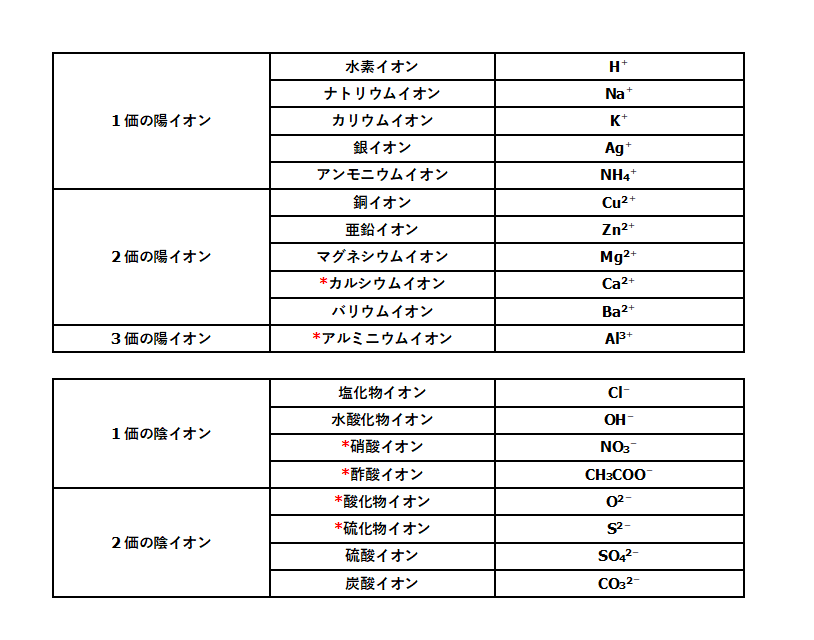



中3化学 イオンとは 中学理科 ポイントまとめと整理
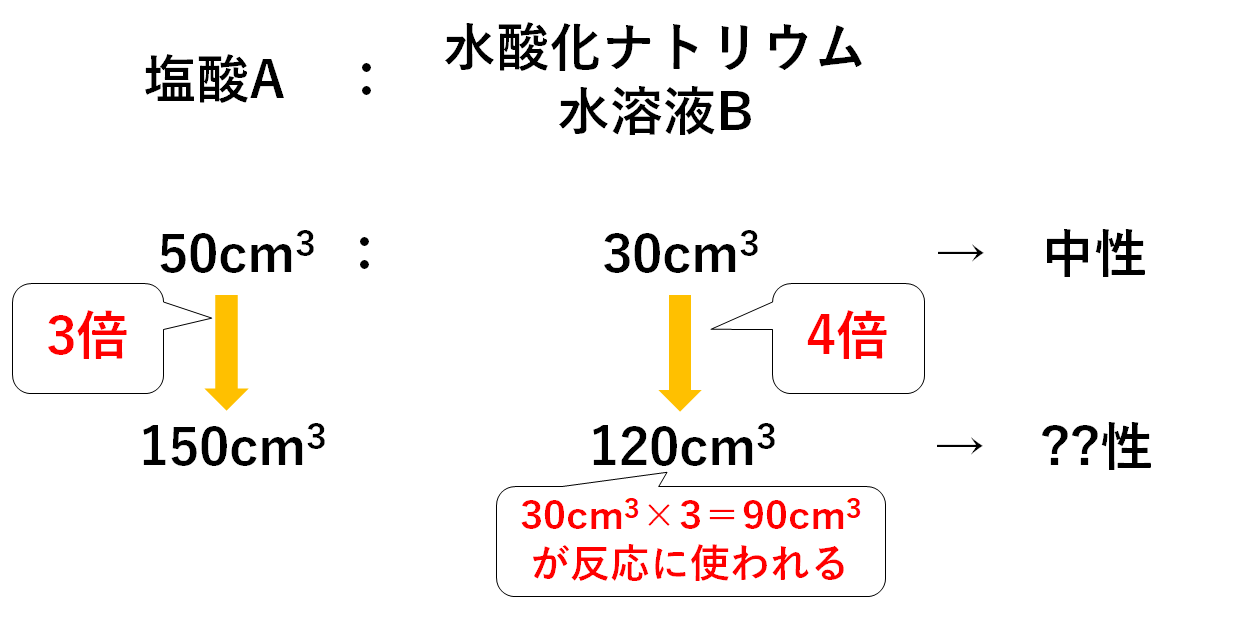



中3化学 中和の量的関係 中学理科 ポイントまとめと整理




中学理科 浮力とグラフの練習問題 なるほどの素




塩化銅水溶液の電気分解をしよう 中学理科3年生 オペラだって あんたがたどこさブログ




中3理科 完全中和の計算 Pikuu




密度の公式 物質の密度の求め方は しみた の法則 中学理科 Yattoke 小 中学生の学習サイト
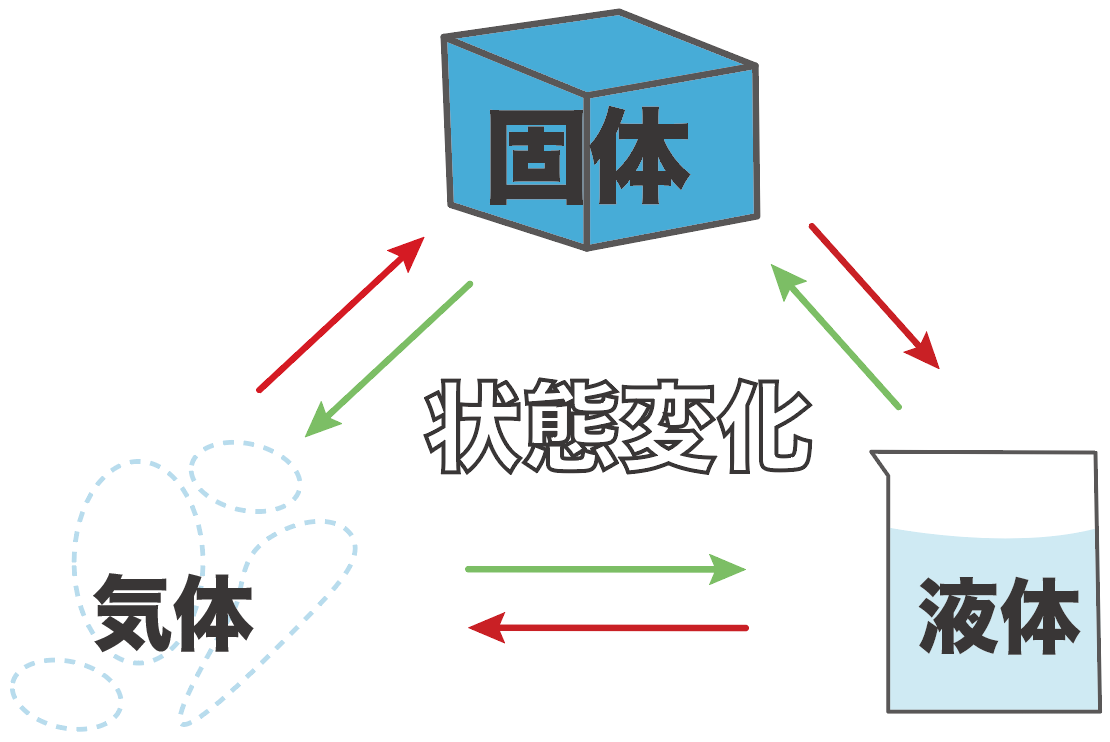



中1理科 3分でわかる 状態変化とは一体何もの Qikeru 学びを楽しくわかりやすく



1




中1理科 金属の3つの性質 練習編 映像授業のtry It トライイット



中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス




中3理科 イオン 酸とアルカリ 中和まとめと問題



Http Www Mct Ne Jp Users Koavc Kon1 Data2 Jh3 Sc 04 Pdf




中学3 理科 イオンのグラフ 下の写真のやり方が分かりません どのよう Okwave




中学理科の私立入試対策まとめ



Fddata中学中間期末過去問集



中3理科 中和の計算問題 Examee




中1理科 密度の単位と計算方法 練習編1 映像授業のtry It トライイット
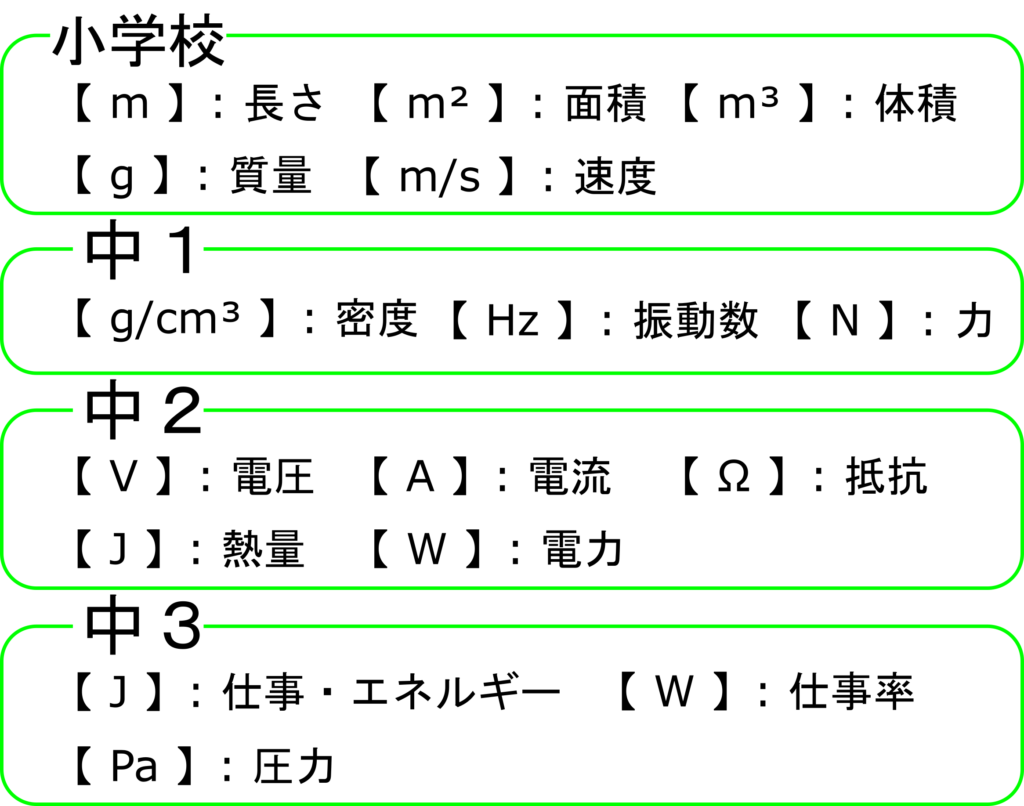



中学理科 単位って何 K キロ やc センチ の意味と単位の変換方法を学ぼう 理科の授業をふりかえる



Search Q E4 B8 Ad1 E7 90 86 E7 91 E6 8d E7 Tbm Isch




理科ノート




中3化学 塩酸の電気分解 知識問題 中学理科の問題パターンと練習問題



中1理科 3分でわかる 水圧 浮力とは何もの Qikeru 学びを楽しくわかりやすく
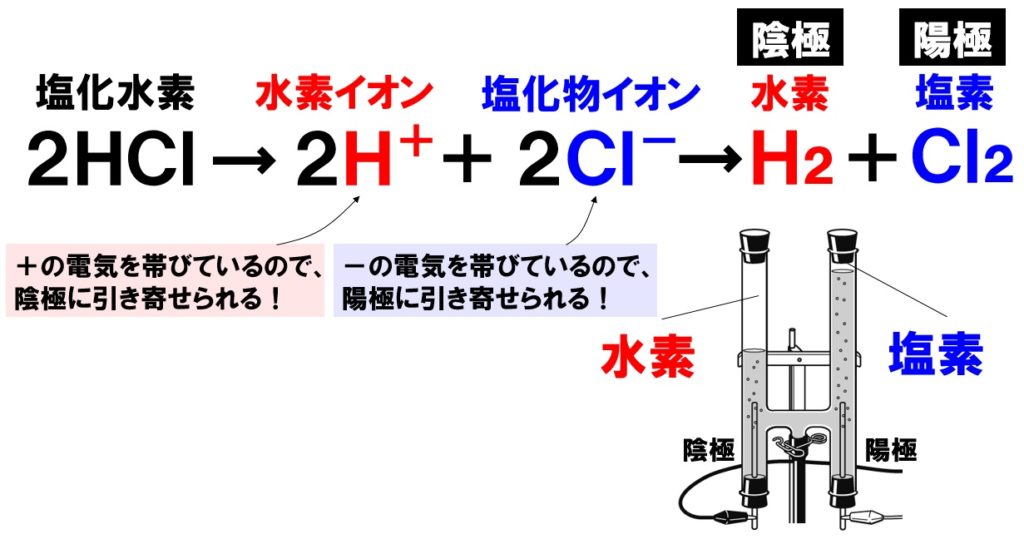



中3理科 塩酸の電気分解のポイント Examee
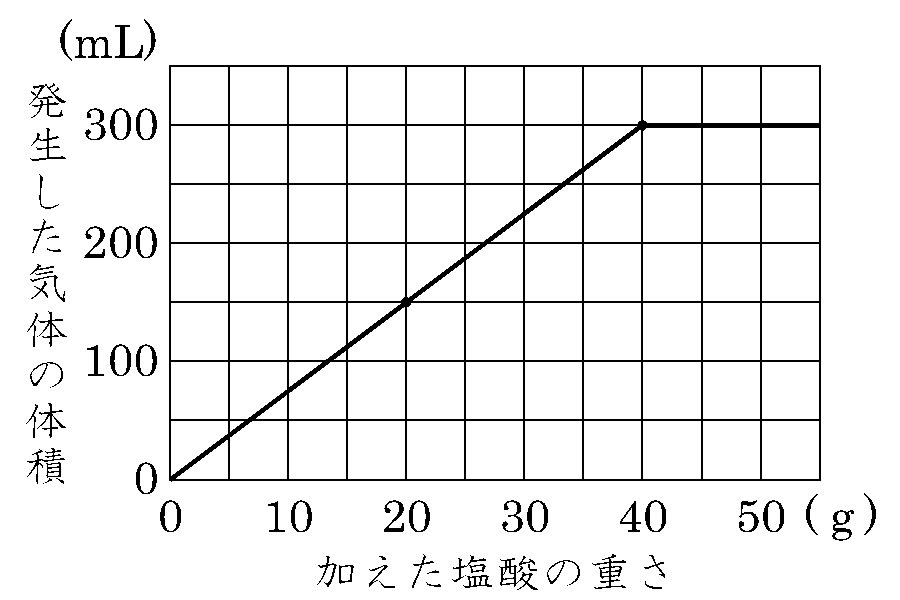



共通テストに出ます 中学三年理科 グラフ 1 べんきょうなせん W




中3理科 酸とアルカリの実験のポイント Examee




中3理科 完全中和の計算 Pikuu



中3理科中和と濃度体積の問題です 助けてください 大問1の 1 しかわかりませ Yahoo 知恵袋



Q Tbn And9gct Rgzxbmqvy7dihzvtztayfctyi9bhvk32viujuihzd0k5mqnv Usqp Cau




中和 問題解説 Youtube




中1理科 メスシリンダーの使い方 映像授業のtry It トライイット



新学習指導要領準拠 チャート式 基礎からの中学理科総仕上げ チャート式の数研出版




中3 理科 2学期 期始め 実力テスト 練習問題 赤城 ᐡᐤᐡ




中3理科です 中和の反応の単元で 水溶液中のイオンの総数と 水溶液の体積をグラフに表 Clear
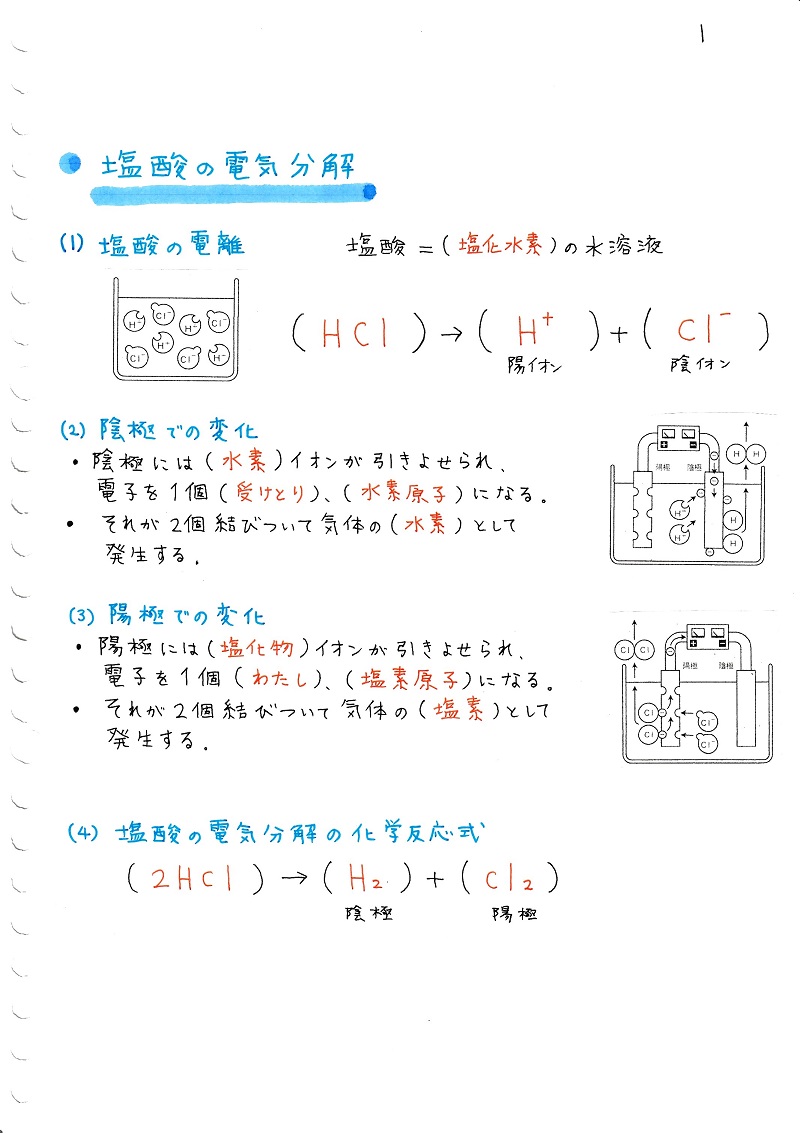



中学理科 水溶液とイオン4 まとめ編 ママ塾ノート



中3理科中和と濃度体積の問題です 助けてください 大問1の 1 しかわかりませ Yahoo 知恵袋




中1理科基本問題集 単元2物質のすがた 化学分野




中1理科基本問題集 単元2物質のすがた 化学分野




Pdf 中和の量的関係 計算ドリル25題 中学理科ポイントまとめと整理 オンラインショップ




21年版 中学生におすすめの 理科 問題集ランキング




Learn De Leon 家庭教師 ランデレオン 理科 計算 公式 密度 質量 体積 فيسبوك




中3理科の学習ポイント 今すぐニガテを克服しよう 家庭教師ジャニアス


